Absorptionsspektrum
Von Gasatomen gestreute Strahlung
Basiswissen
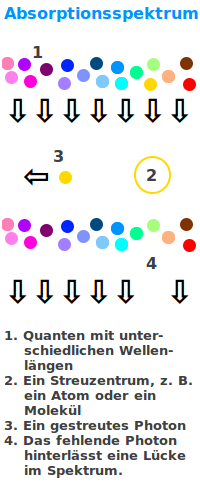
Ein bunter Streifen fließend ineinander übergehender Farben mit einigen schwarzen Strichen dazwischen: das ist das typische Bild für ein Absorptionsspektrum. Bestimmte Wellenlängen elektromagnetischer Strahlung die in einem Spektrum fehlen bilden das Muster aus schwarzen Linien. Das sind die fehlender Wellenlängen. Die Gesamtheit dieses Musters ist das Absorptionsspektrum.
Wie entsteht ein Absorptionsspektrum?
Atome haben Elektronen in ihrer Hülle. Einzelne Elektronen in der Atomhülle können von außerhalb des Atoms Energie aufnehmen und diese später wieder abgeben. Die Elektronen bestimmter Atomsorten nehmen dabei die Energie immer nur in Form bestimmter elektromagnetischer Wellen mit immer gleicher Wellenlänge ab (Franck-Hertz-Versuch). Wird ein Gas mit Licht eines kontinuierlichen Spektrum (alle Farben) angestrahlt, werden die absoprtionsfähigen Wellenlängen von den Gasatomen geschluckt und anschließend wieder ausgesandt. Die Aussendung erfolgt aber nicht mehr notwendigerweise in die vorherige Ausbreitungsrichtung des Lichts. Die Aussendung erfolgt zufällig in irgendeine Richtung. Dadurch fehlt Licht dieser Wellenlänge in der vorherigen Ausbreitungsrichtung. Betrachtet man das so angestrahlte Gas, fehlen also bestimmte Farben. Das so entstandene Spektrum nennt man ein Absorptionsspektrum.
Das Sonnenspektrum als klassisches Absorptionsspektrum
Ein typisches Absorptionsspektrum bildet das Licht von der Sonne: An der Sonnenoberfläche verlässt Licht die Sonnenkugel. Um die Sonne gibt es eine Hülle aus Gasen, die sogenannte Photosphäre. In ihr gibt es unter anderem Wasserstoff-, Helium-, Sauerstoff-, Kohlenstoff- und Eisenatome. Diese Atome verursachen für die Sonne typische schwarze Linien in einem Spektrum. In einem Spektroskop sieht man einen kontinuierlichen Streifen ineinander übergehende bunter Farben. Dazwischen gibt es jedoch schmale schwarze Lücken. Das ganze ist das Absorptionsspektrum. Das klassische Beispiel für ein Absorptionsspektrum sind die Fraunhoferlinien ↗
Wellenlänge oder Frequenz?
- Es wird oft wahlweise von Frequenz oder Wellenlänge gesprochen.
- Zu einer bestimmten Frequenz gehört immer eindeutig eine feste Wellenlänge.
- Man kann sagen: Wellenlänge ist eine Funktion der Frequenz.
- Es gilt die Umrechnungsformeln: c = l·f
- c = Lichtgeschwindigkeit
- l = Wellenlänge
- f = Frequenz
Abgrenzung
Neben dem Absorptionsspektrum spricht man auch von einem Emissionsspektrum. Die Elektronen in der Atomhülle nehmen elektromagnetische Strahlung nicht nur in festgelegten Wellenlängen auf, sondern sie geben sie auch nur in diesen atomsortenspezifischen Wellenlängen wieder ab. Dieser Effekt führt im Elektroskop zu einzeln leuchtenden Streifen, ein sogenanntes Emissionsspektrum ↗
Beispiel
- Das klassische Beispiel ist das Absorptionsspektrum der Sonne.
- Im kontinuierlichen Spektrum des Sonnenlichts fehlen über 500 Wellenlängen.
- Mehr dazu unter Fraunhoferlinien ↗